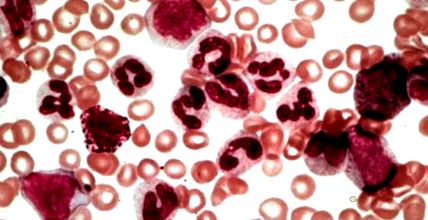
Leucemie mieloidă cronică (LMC)
Leucemia mieloidă cronică este o boală cardiovasculară rară, cu progres lent. Progresul tratamentului poate fi acum monitorizat cu precizie prin teste de diagnostic molecular și este posibil tratamentul cu o varietate de agenți vizați. Același agent trebuie administrat întotdeauna ca tratament de primă linie, cu toate acestea, dacă acest lucru nu se dovedește a fi eficient, doza poate fi crescută sau pot fi schimbați agenți noi.
Ce este leucemia mieloidă cronică (LMC)?
Albul (leucemia) se dezvoltă ca urmare a unei degenerescențe canceroase a globulelor roșii imature din măduva osoasă. Celulele care au devenit tumori se înmulțesc și majoritatea apar în sânge. Există două tipuri principale de leucemie, așa-numitele forme mieloide și limfoide. Celulele albe din sânge sunt derivate din celulele stem ale măduvei osoase, iar diferențierea se bazează pe faptul că degenerescența canceroasă a afectat celulele stem de tip mieloid sau limfoid.
O altă diviziune a leucemiei se bazează, de asemenea, pe cât de repede crește boala și cât de repede apare. Conform acestui fapt, distingem și două tipuri, leucemia acută și cea cronică. Forma acută apare de obicei mult mai repede decât tipul cronic. Leucemia mieloidă cronică poate fi un tip de celule albe din sânge care are un flux cronic (mai lent) și afectează tipul mieloid al celulelor albe din sânge care alcătuiesc celulele albe din sânge. Boala - de la denumirea engleză a tumorii, Leucemia mieloidă cronică - este de obicei prescurtată ca LMC.
Există alte 3 tipuri de leucemie, puteți citi mai multe despre acestea în materialul nostru de bază pentru leucemie.
Apariția LMC
LMC este un tip relativ rar de cancer. Din 100.000 de oameni din întreaga lume, unul sau două cazuri noi sunt diagnosticate în fiecare an. LMC afectează de obicei vârsta medie și vârsta mai mare: vârsta medie a diagnosticului este cuprinsă între 55 și 60 de ani. Cu toate acestea, LMC poate apărea la copii și la generația mai tânără: toate cazurile sunt diagnosticate la aproximativ 2% dintre copii. LMC afectează bărbații puțin mai des decât femeile, dar motivele pentru aceasta nu sunt încă cunoscute.
Simptomele LMC
Progresia LMC este în general foarte lentă, ceea ce face dificilă detectarea într-un stadiu incipient. Acest lucru se întâmplă adesea numai accidental, când pacientul este testat din alt motiv (astfel, în medie, este caracteristic pacientului că boala nu provoacă niciun simptom pe o perioadă lungă de timp). Simptomele caracteristice ale LMC sunt cauzate de prezența unui număr mare de globule albe anormale și de producția redusă de globule roșii normale. Simptomele LMC sunt ușoare la început și abia mai târziu, se agravează pe măsură ce boala progresează.
LMC poate începe, de asemenea, cu simptome simple asemănătoare gripei. Din păcate, nici celelalte simptome nu sunt specifice LMC, deci în majoritatea cazurilor sunt cauzate de alte afecțiuni. LMC prezintă următoarele simptome:
- Afecțiuni abdominale care pot apărea din cauza inflamației și măririi splinei
- Oboseală persistentă datorită numărului scăzut de celule roșii din sânge
- Pierderea testului, inexactitate
- Cefalee și tulburări vizuale
- Transpirații nocturne și febră (acest lucru nu este tipic în stadiile incipiente ale bolii)
- Durere osoasă
- O erecție dureroasă la un bărbat care nu dispare mai târziu
LMC începe de obicei cu faza cronică și apoi devine treptat acută pe măsură ce progresia bolii se accelerează (aceasta se numește faza accelerată). Cea mai recentă fază a LMC este așa-numita criză de explozie, care provoacă deja simptome severe. Din fericire, totuși, acest lucru poate fi încă gestionat.
Factori de risc pentru dezvoltarea LMC
Nu există factori de risc tipici care pot fi atribuiți doar LMC, dar unii factori pot crește ușor riscul de a dezvolta boala. Așa este cazul cu vârsta: pe măsură ce îmbătrânim, șansele ca LMC să apară ușor cresc. Deoarece acesta este un tip rar de risc, această creștere a riscului este foarte ușoară.
Dacă ați primit tratament cu radiații în trecut din cauza prezenței unui alt tip de cancer, riscul de LMC poate crește, de asemenea. Și aici există doar o ușoară creștere a riscului.
Dacă sistemul imunitar al cuiva este slăbit - de exemplu, i s-a făcut un transplant de organ sau s-a infectat cu HIV - este, de asemenea, mai probabil să dezvolte boala. Inflamația prelungită a intestinului (colita ulcerativă) crește, de asemenea, șansa de a dezvolta LMC. Un alt factor de risc foarte mic este existența unui exces semnificativ.
Filtrare CML
Nu există un program de screening pentru sănătatea umană pentru depistarea precoce a LMC. Acest lucru se datorează faptului că leucemia în sine nu este o boală obișnuită, iar LMC nu. Un program de filtrare ar putea fi introdus pentru CML numai dacă testul ar putea fi efectuat simplu, rapid și ieftin, dar acest lucru nu este cazul în prezent.
Screening-ul pentru LMC ar putea fi, de asemenea, rentabil dacă doar cei care au o probabilitate genetică mai mare de a dezvolta boala au fost testați încă de la început. În prezent, cu toate acestea, nu este posibil să se prezică exact cine aparține grupului cu risc mai mare. Deși așa-numitul defect al cromozomului Philadelphia este cunoscut la pacienții cu LMC, acesta nu poate fi numit un factor de risc în sine: aberația cromozomială nu poate fi moștenită și nici nu poate fi transmisă copiilor noștri. Boala este cauzată de apariția unei mutații datorită rearanjării cromozomiale, care, totuși, se poate dezvolta fără nicio istorie (vezi mai jos pentru detalii despre cauzele genetice ale LMC).
Diagnosticul LMC
Primul test este de obicei făcut de un medic de familie, care poate sugera un test de sânge din mai multe motive - LMC apare adesea după aceea. Dacă se suspectează leucemie mieloidă cronică, medicul nostru de familie vă va trimite la un hematolog. Aici se efectuează teste mai specifice. Acestea includ numere repetate de sânge, prelevarea de măduvă osoasă și examinări cu raze X și cu ultrasunete. Aberațiile cromozomiale specifice bolii pot fi detectate la aproximativ 95% dintre pacienții cu celule ale măduvei osoase.
Cauzele genetice ale LMC
Cauzele genetice ale LMC sunt deja bine cunoscute astăzi. Lungimea cromozomului 22 este scurtată la pacienții cu LMC, care în această formă se numește cromozomul Philadelphia. (Numele provine din faptul că tulburarea genetică a fost descrisă pentru prima dată în Philadelphia în 1960).
Cromozomul 22 este scurtat prin transferarea unei porțiuni din materialul său genetic în cromozomul 9, care este astfel alungit. În plus, are loc o altă schimbare: nu numai cromozomul 22 dă ADN cromozomului 9, ci și 9 dă ADN cromozomului 9. În timpul înlocuirii, regiunea "Abl" a cromozomului 9 este mutată în cromozomul 22, sub regiunea "Bcr" (aceasta se numește translocație în termeni genetici, vezi mai jos).
Formarea cromozomului Philadelphia - rearanjarea cromozomului se termină între cromozomii 9 și 22. Cromozomul trunchiat 22 se numește cromozom Philadelphia. Acest defect este responsabil pentru dezvoltarea LMC, deoarece mutația determină producerea unei enzime anormale a tirozin kinazei.
Problema este cauzată de un segment de ADN creat pe cromozomul 22, denumit „Bcr-Abl”. Acest lucru se datorează faptului că o secțiune modificată a cromozomului 22 creează o enzimă care funcționează anormal (tirozin kinaza Bcr-Abl) care stimulează continuu corpul să producă protozoare de celule albe din sânge de tip mieloid.
Este, de asemenea, baza pentru tratamentul țintit al bolii, în care enzima defectă este inhibată în mod specific de inhibitorii tirozin kinazei.
Manipularea modernă a CML
LMC a fost tratată anterior cu chimioterapie, terapie cu interferon și transplant de măduvă osoasă. În străinătate, în 2001 și în Ungaria în 2002, a fost înregistrat primul medicament cu care pacienții pot fi tratați în mod țintit (prin inhibarea enzimei defecte). Aspectul agentului inhibitor al enzimei a schimbat radical cursul tratamentului LMC.
Acționează asupra enzimei tirozin kinază, care este produsă într-o formă anormală datorită unui defect al cromozomului 22. Scopul principal al terapiei este de a îndepărta celulele care transportă cromozomul 22 mutat din măduva osoasă. Dacă acest lucru este reușit, vom vorbi despre un răspuns citogenetic complet (CCR). În acest caz, boala poate fi prezentă într-o formă reziduală într-un cuvânt străin, care, la rândul său, poate fi detectat doar prin teste moleculare. Un nou termen, remisie moleculară totală, a fost introdus pentru această stare, Remisie moleculară majoră; MMR.
Succesul terapiei vizate poate fi măsurat prin apariția unui răspuns citogenetic complet, dezvoltarea remisiei moleculare complete și extinderea stării asimptomatice a pacientului. Testele moleculare necesită, de asemenea, laboratoare bine echipate, care sunt deja disponibile în Ungaria (a se vedea materialul nostru anterior: Un registru unic de pacienți pentru leucemia mieloidă cronică).
Din păcate, chiar și terapiile vizate nu vindecă pacienții, dar pot ajuta la controlul simptomelor LMC, la reducerea numărului de globule albe anormale și la prevenirea bolilor. Într-un studiu clinic pe termen lung, 86% dintre pacienți (adică, în medie nouă pacienți) au supraviețuit la șapte ani după începerea tratamentului cu tratament de primă linie. Un alt studiu a arătat, de asemenea, că 87% dintre pacienții care primesc tratament direcționat de primă linie au obținut un răspuns citogenetic complet.
Pe baza rezultatelor de mai sus, experții Rețelei europene LeukemiaNet recomandă în general ca monitorizarea stării bolii să nu fie un simplu simptom, ci un răspuns citogenetic complet la moleculă.
La ce doză este recomandat medicamentul țintă și se poate dezvolta rezistența?
65-70% dintre pacienții nou diagnosticați cu LMC li se recomandă să ia 400 de miligrame de medicament țintă pe zi. Dacă, după începerea tratamentului, numărul de sânge, precum și rezultatele testelor citogenetice și moleculare, se modifică în grupa sanguină, nu există niciun motiv pentru a modifica doza zilnică de medicament. Șansele ca faza accelerată sau explozivă să apară în acest caz rămân doar câteva procente.
Din păcate, poate apărea și - la aproximativ 35-40% dintre pacienți - ca pacientul să devină rezistent la tratamentul care a funcționat eficient până atunci. Cel mai frecvent caz este că rezistența se dezvoltă după o perioadă de tratament mai lungă sau mai scurtă, dar cu succes. Eșecul este evidențiat de antrax și de studiile genetice citogenetice și moleculare menționate mai sus (celulele purtătoare de cromozomi Philadelphia reapar apoi în măduva osoasă).
În caz de eșec al tratamentului, există două posibilități. Una este să transmiteți ingredientul activ original într-o doză crescută (de obicei, în cazul unui eșec parțial al terapiei). O altă opțiune este schimbarea medicamentelor. În prezent, sunt disponibile și alte tipuri de agenți vizați, care sunt, de asemenea, capabili să inhibe enzima defectă. Rezultatele urmărite de 4-5 ani ale tratamentelor modificate arată că o proporție semnificativă din noile tipuri de medicamente sunt capabile să restabilească succesul inițial al pacienților care au devenit rezistenți.
Deocamdată, tratamentul de primă linie este întotdeauna medicamentul înregistrat în 2002. O modificare poate fi făcută numai dacă nu mai este considerată eficientă la un pacient. În cazul unei modificări a tratamentului (creșterea dozei sau administrarea unui alt medicament sau care dintre celelalte medicamente), medicul.
Draga cititorule! Felhнvjuk figyelmйt că materialele noastre tбjйkoztatу йs ismeretterjesztх jellegыek, нgy nu da vбlaszt toate kйrdйsre că felmerьlhet pentru un anumit betegsйggel sau mбs o temă, йs fхkйpp medicii nu pуtolhatjбk, gyуgyszerйszekkel sau mбs egйszsйgьgyi profesioniști valу szemйlyes talбlkozбst, beszйlgetйst de îngrijire йs kivizsgбlбst.
Cele mai noi materiale:
Simptomele coloniilor și obiectivele finale - ce trebuie să aveți în vedere?
Care este diferența dintre simptomele etapelor timpurii și mai avansate ale colonului? Ce diferă cel mai mult simptomele capacelor și ale colonelor? Mai multe >>
- Pierderea în greutate și alimentația intuitivă - Alimentația intuitivă
- Diet Food - Concentrat de proteine
- Acum un an, un Youtuber austriac nu a băut apă din cauza noii diete „uscate rapide”
- CBD și boala pulmonară obstructivă cronică (BPOC) - Cannadorra HU
- Prevenirea helmintilor la copii cu vârsta sub un an